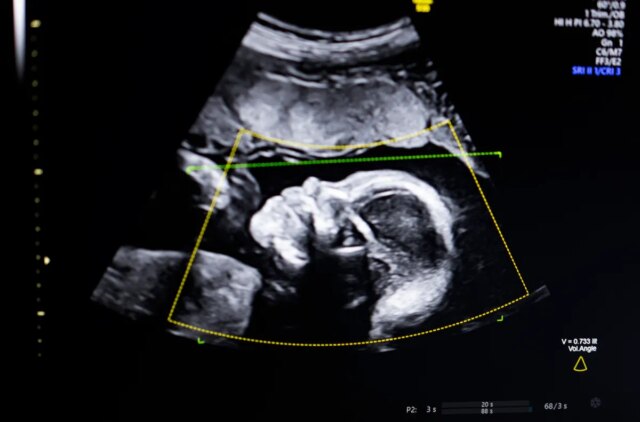
Il vincitore del TechCrunch Disrupt Battlefield 2023, Biotics AI, ha annunciato lunedì di aver ricevuto l’approvazione della FDA per il suo software program AI che aiuta a rilevare anomalie fetali nelle immagini ecografiche.
Il prodotto è stato ideato dal fondatore e CEO Robhy Bustami, cresciuto in una famiglia di ostetrici, tra cui sua madre, sua sorella e suo zio. Ha trascorso molto tempo negli ospedali crescendo, spesso viaggiando con sua madre mentre forniva assistenza materna in tutti gli Stati Uniti
Dopo aver imparato a programmare e aver studiato informatica alla UC Irvine, Bustami ha collaborato con Salam Khan, Chaskin Saroff e il dottor Hisham Elgammal nel 2021 per lanciare Biotics AI,
La tecnologia utilizza l’intelligenza artificiale della visione artificiale “per supportare la valutazione della qualità dell’ecografia fetale, la completezza anatomica, il reporting automatizzato e l’integrazione perfetta nei flussi di lavoro clinici”, ha dichiarato Bustami a TechCrunch.
Spera che la sua tecnologia aiuti gli Stati Uniti a combattere il fatto che gli Stati Uniti hanno uno dei peggiori esiti prenatali per le madri tra le nazioni ad alto reddito. Le donne nere, in particolare, devono affrontare un tasso molto elevato di morti materne,
Bustami ha affermato che l’ecografia prenatale è diventata la “pietra angolare” del monitoraggio delle gravidanze, ma le sue immagini di bassa qualità possono portare a diagnosi errate.
Bustami ha affermato che la parte più difficile non è stata costruire i suoi modelli di intelligenza artificiale, che sono stati addestrati su una serie diversificata di 11.000 ultrasuoni, ma garantire che la tecnologia funzionasse in modo affidabile nel mondo reale, in particolare sui dati demografici con il rischio più elevato di un esito tragico.
Evento Techcrunch
San Francisco
|
13-15 ottobre 2026
“In un ambiente in cui le disparità nei risultati sanitari sono ben documentate, period fondamentale dimostrare prestazioni coerenti tra i sottogruppi di pazienti, non solo nei casi idealizzati”, ha continuato Bustami.
Il CEO ha affermato che ci sono voluti poco meno di tre anni per completare il processo della FDA, compresi i take a look at e la convalida del prodotto. L’esperienza ha insegnato a lui e al suo group quanto sia fondamentale che il lavoro di ingegneria, prodotto, clinico e normativo sia strettamente allineato fin dall’inizio. “Progettando il prodotto, la validazione clinica e il percorso normativo insieme, anziché in sequenza, siamo stati in grado di agire rapidamente”, ha affermato.
Ora che la FDA ha ottenuto l’autorizzazione, Bustami ha affermato che il prossimo obiettivo delle aziende sarà quello di estendersi a vari sistemi sanitari a livello nazionale. Ha inoltre in programma di aggiungere ulteriori funzionalità per la medicina fetale e la salute riproduttiva.
“Siamo nella posizione di poter ampliare sia la distribuzione che l’impatto clinico, continuando advert approfondire la potenza della nostra tecnologia”, ha affermato.